Co je NMN?
- Popisky, shora:
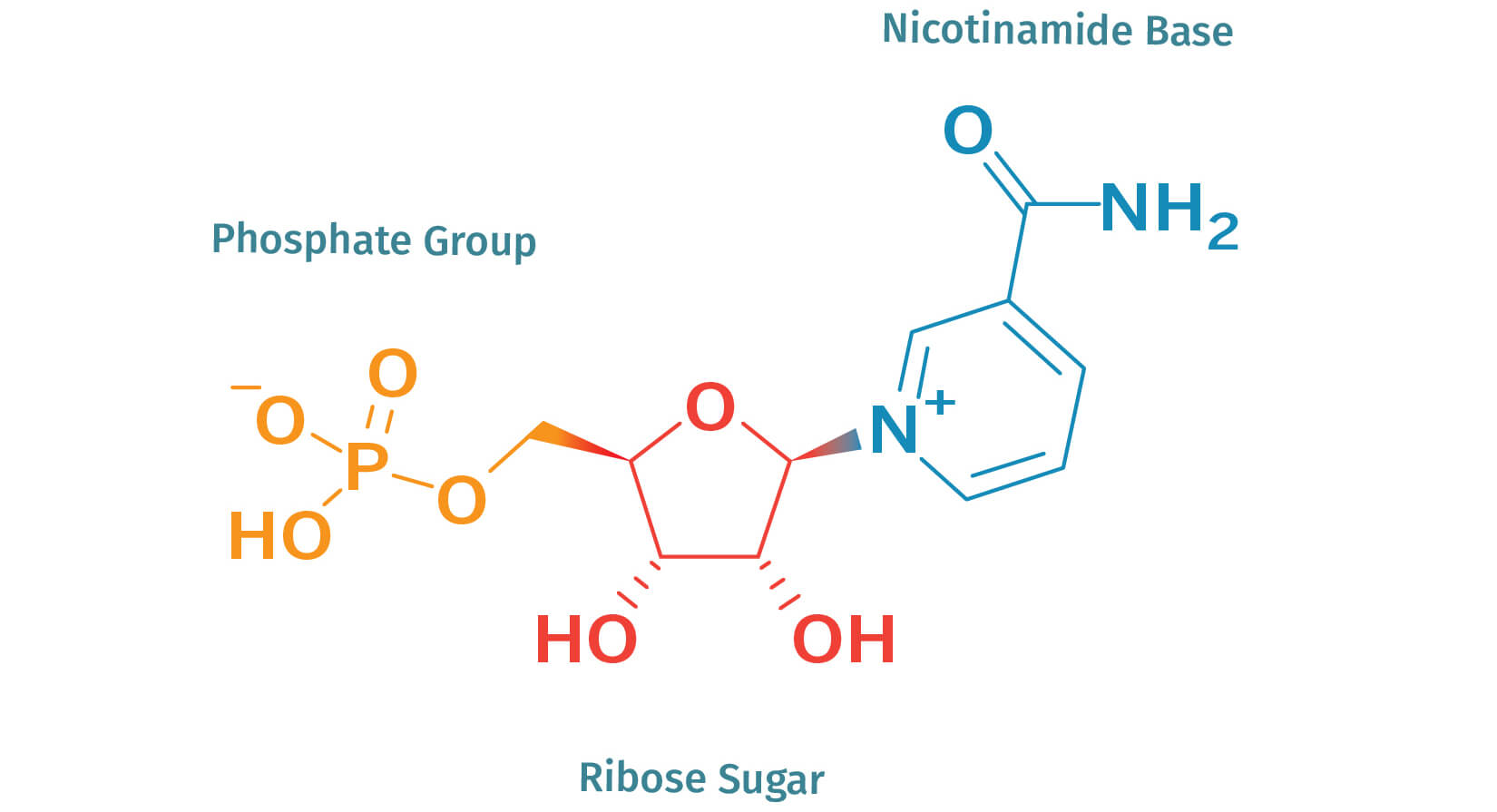
- Nikotinamidová báze
- Fosfátová skupina
- Ribózový cukr
NMN je zkratka názvu nikotinamid mononukleotid, molekula, která se přirozeně vyskytuje ve všech formách života. Na molekulární úrovni se jedná o ribonukleotid, což je základní stavební jednotka nukleové kyseliny RNA. Strukturálně se molekula skládá z nikotinamidové skupiny, ribózy a fosfátové skupiny (Obr. 1). NMN je přímým prekurzorem esenciální molekuly nikotinamidadenindinukleotidu (NAD+) a je považován za klíčovou látku zvyšující koncentraci NAD+ v buňkách.
Co je nikotinamidadenindinukleotid (NAD+)?
NAD+ je esenciální koenzym nezbytný pro život a všechny buněčné funkce. Enzymy jsou katalyzátory, které umožňují biochemické reakce. Koenzymy jsou „pomocné“ molekuly nezbytné pro to, aby mohly enzymy fungovat.
Jakou má NAD+ funkci?
NAD+ je nejčetněji zastoupenou molekulou v těle hned po vodě, a bez něj by organismus zahynul. NAD+ využívá řada bílkovin v celém těle, jako jsou například sirtuiny, které opravují poškozenou DNA. Je významný také pro mitochondrie, což jsou buněčné elektrárny generující chemickou energii, kterou potřebuje naše tělo pro život.
Funkce NAD+ jako koenzymu u mitochondrií
NAD+ hraje obzvláště významnou roli v metabolických procesech, jako je glykolýza, TCA cyklus (známý také jako Krebsův cyklus nebo cyklus kyseliny citrónové), v elektronovém transportním řetězci, který probíhá uvnitř našich mitochondrií a je způsobem, jak naše buňky získávají energii.
Ve své roli ligandu se NAD+ váže na enzymy a přenáší elektrony mezi molekulami. Elektrony jsou atomární bází buněčné energie a přenosem z jedné molekuly do druhé NAD+ realizuje buněčný mechanismus podobný dobíjení baterie. Baterie je vybitá tehdy, když jsou spotřebovány elektrony, které dodávají energii. Bez potřebné podpory se tyto elektrony nemohou vrátit do svého výchozího místa. V buňkách má NAD+ roli právě takového podpůrného prvku. Tímto způsobem dokáže NAD+ snižovat nebo zvyšovat aktivitu enzymů, expresi genů a signalizaci buněk.
NAD+ pomáhá kontrolovat poškození DNA
Jak organismy stárnou, jejich DNA se postupně poškozuje v důsledku působení faktorů prostředí, jako je radiace, znečištění a nepřesná replikace DNA. Podle současné teorie stárnutí je nahromadění závad v DNA hlavní příčinou stárnutí. Téměř všechny buňky obsahují „molekulární mechanismus“ pro opravu těchto poškození. Tento mechanismus spotřebovává molekuly NAD+ a energii. Rozsáhlé poškození DNA proto může vyčerpávat cenné buněčné zdroje energie.
Na NAD+ závisí funkce jedné z bílkovin, která je velmi důležitá právě pro opravy DNA – PARP (poly (ADP-ribóza) polymeráza). Starší lidé mají snížené hladiny NAD+. Nahromadění poškození DNA je výsledkem běžného procesu stárnutí a vede ke zvýšení hladiny PARP. V důsledku toho se snižuje koncentrace NAD+. Toto vyčerpání zásob se pak dále prohlubuje při jakémkoli dalším poškození DNA v mitochondriích.
PARP1 je „zprostředkovatelem“ opravy DNA
Popisky
- vlevo, shora:
- NAD+
- Vazebné místo
- Automodifikační doména
- Doména vazby DNA
- vpravo, shora:
- PŘITAHUJE OPRAVNÉ MECHANISMY PRO:
- - Přerušení na jednom vlákně
- - Adukci DNA, tj. vazbu DNA na rakovinotvorné látky
- - Replikační léze, tj. poškození báze DNA, deleci báze, alteraci nukleotidu, případně přerušení vlákna
Schéma, jak PARP1 pomáhá opravovat poškozenou DNA
Popisky
- Ligáza 3
- PARP-1 opravuje poškozenou DNA
- - Lehké nebo chemické poškození DNA
- - Ligáza 3 a NAD+ vážou DNA
Jak NAD+ ovlivňuje aktivitu sirtuinů (genů dlouhověkosti)?
Popisky, horní část
- Aktivace!
- Stáří Přežití Opravy DNA Metabolismus
- Mozek / CNS
- Neurodegenerace
- Srdce
- Zánět
- Ochrana srdce
- Játra
- Oxidace mastných kyselin
- Glukoneogeneze
- Tuk
- Lipogeneze
- Slinivka
- Sekrece inzulinu
- Kosterní svaly
- Inzulinová senzitivita
- Oxidace mastných kyselin
Nově objevené sirtuiny, známé také jako „strážci genů“, hrají zásadní roli v udržování zdraví buněk. Sirtuiny patří do rodiny enzymů, účastní se reakcí na buněčný stres a oprav poškození. Zapojují se také do sekrece inzulinu, procesů stárnutí a různých stavů souvisejících s věkem, jako jsou například neurodegenerativní onemocnění a diabetes. Aktivace sirtuinů je závislá na NAD+.
Jak říká David Sinclair, harvardský genetik a vědec zkoumající NAD, ztrácíme NAD+ spolu s tím, jak stárneme, a „z toho plynoucí pokles aktivity sirtuinu je považován za primární příčinu onemocnění, která přicházejí ve věku, kdy ještě nejsme staří, ale kdy už nejsme ani mladí.“ Věří, že přirozené zvyšování NAD+ s přibývajícím věkem dokáže zpomalit nebo zvrátit určité procesy stárnutí.
Proč bychom se měli zajímat o NAD+
Od objevu NAD+ v roce 1906 byla tato molekula v hledáčku vědců pro její četnost v těle a pro klíčovou roli v molekulárních procesech, které udržují naše tělo v chodu. Ve studiích na zvířatech prokázalo zvýšení NAD+ slibné výsledky například při výzkumu metabolických procesů nebo nemocí souvisejících s věkem. Zjistilo se také, že molekula má vlastnosti zpomalující stárnutí a oddalující propuknutí nemocí souvisejících s věkem, jako je například diabetes, kardiovaskulární onemocnění, neurodegenerace a obecně snížení aktivity imunitního systému.
Může NMN pomoci v boji s COVID-19?
Spolu s tím, jak se COVID-19 prohnal celým světem, kde infikoval milióny lidí a vyvolával onemocnění s příznaky zápalu plic, pustili se vědci do hledání bezpečné a účinné léčby. Gerontologové, vědci, kteří studují biologii stárnutí, věří, že léky cílící právě na procesy stárnutí mohou poskytnout nový úhel pohledu na řešení současné pandemie.
Statistiky ukázaly, že COVID-19 infikuje převážně starší populaci. Přibližně 13,4 % pacientů ve věku 80 let a více zemře na COVID-19 v porovnání s pouhým 1,25 % a 0,06 % osob v 50. a 20. letech života. Nedávná studie Oxfordské univerzity, analyzující 17.4 milionů obyvatel Velké Británie, prokázala, že věk je nejzávažnějším rizikovým faktorem spojovaným s úmrtím na COVID-19. Další rizikové faktory zahrnovaly mužské pohlaví, neřešený diabetes a těžké astma.
Vzhledem k této povaze viru, kdy ohrožuje především starší osoby, jsou někteří gerontologové toho názoru, že léčba „stárnutí“ by mohla být dlouhodobým řešením v ochraně starších lidí před onemocněním COVID-19 a dalšími infekcemi, které se mohou vyskytnout v budoucnu. Ačkoli je stále třeba provést další výzkumy, nedávná studie uvedla látky posilující NAD+, jako je NMN a NR mezi možnostmi potenciální léčby. Další vědci vyslovili hypotézu, že starší lidé mohou mít prospěch z účinků NAD+ na podporu dlouhověkosti a předejít fatální extrémní aktivaci imunitní odezvy, označované jako cytokinová bouře, při níž tělo napadá spíše své vlastní buňky než samotný virus.
Na základě současné studie, která ještě neprošla recenzním řízením, buňka v boji proti koronaviru spotřebovává NAD+ , čímž oslabuje tělo. NAD+ je nezbytný pro přirozenou imunitní obranu proti virům. V rámci této studie se výzkumníci snaží posoudit, zda mohou posilovače NAD+ pomoci porazit pandemii.
Zatím, co se vědci v laboratořích snaží porazit čas a najít lék na COVID-19, lékaři v první linii vyčerpávají dostupné možnosti a obracejí se k inovativním postupům. Jako poslední naději pro své pacienty zvolil doktor Robert Huizenga z kliniky Cedars Sinai podání koktejlu NMN doplněnému boostery, jako je například zinek, svým pacientům s cílem zmírnit cytokinovou bouři rozpoutanou COVID-19. NMN koktejl pacientům snížil horečku a zánětlivé projevy již během 12 hodin po podání.
Při této pandemii se NMN dostává stále více pozornosti pro jeho roli v udržování rovnováhy imunitního systému, což může být možné řešení cytokinové bouře vyvolané koronavirem. Při předběžných studiích byly zjištěny určité pozitivní výsledky, a ačkoli se ještě nejedná o garantovanou léčbu, řada lékařů a vědců věří, že účinky boosterů NAD+ na COVID-19 stojí za bližší prozkoumání.
Stárnutí
NAD+ je palivo, které pomáhá sirtuinům udržovat integritu genomu a podporovat opravy DNA . Stejně jako auto nemůže fungovat bez pohonných hmot, tak i k aktivaci sirtuinů je potřeba NAD+. Výsledky studií na živočišných modelech prokázaly, že zvyšování koncentrace NAD+ aktivují sirtuiny a zvyšují délku života kvasinek, červů a myší. Ačkoli studie na zvířatech naznačily slibné výsledky proti stárnutí, vědci stále ještě pracují na tom, jak tyto výsledky převést na aplikace pro člověka.
Metabolické poruchy
NAD+ je jedním z klíčů k udržování zdravých mitochondriálních funkcí a stabilního výdeje energie. Stárnutí a strava s vysokým obsahem tuků snižují hladinu NAD+ v těle. Studie prokázaly, že užívání látek podporujících NAD+ (boosterů) mohou zmírnit sklony k přibývání na váze související se stravou a s věkem u myší a zvýšit jejich fyzickou kapacitu, a to i v případě myší staršího věku. Jiné studie zjistily, že tyto látky dovedou dokonce zvrátit účinky diabetu u myších samiček, čímž se otevírají možnosti pro nové strategie boje s metabolickými onemocněními, jakým je například obezita.
Činnost srdce
Podpora koncentrace NAD+ ochraňuje srdce a zlepšuje jeho funkci. Vysoký krevní tlak může vést ke zvětšení srdce a zablokování tepen s následkem mrtvice. U myší dokázaly boostery NAD+ doplnit koncentrace NAD+ v srdci a předcházet jeho poškození vyvolaným nedostatečnou cirkulací krve. Jiné studie prokázaly, že boostery NAD+ chrání myši před abnormálním zvětšením srdce.
Neurodegenerace
U myší s Alzheimerovou chorobou vede zvýšení koncentrace NAD+ k omezení hromadění bílkovin, které narušují komunikaci buněk v mozku, a díky tomu dochází k zlepšení kognitivních funkcí. Posilování koncentrací NAD+ také chrání mozkové buňky před smrtí v situaci, kdy je nedostatečný průtok krve do mozku. Mnoho studií na zvířecích modelech ukazuje nové možnosti pomáhat mozku stárnout zdravě, zabraňovat neurodegeneraci a zlepšovat paměť.
Imunitní systém
Jak stárneme, imunitní systém slábne. Lidé tak snáze onemocní a je stále obtížnější vrátit se z nemoci zpět do plného zdraví, což je patrné zejména u sezónní chřipky nebo u COVID-19. Nedávné studie ukázaly, že koncentrace NAD+ hrají významnou roli v regulaci zánětu a přežití buněk vlivem imunitní reakce a stárnutí. Studie zdůraznila léčebný potenciál NAD+ při dysfunkcích imunity.
Jak tělo vyrábí nikotinamidadenindinukleotid (NAD+)?
Naše těla produkují NAD+ přirozenou cestou z menších komponent neboli prekurzorů. Představte si je jako jakési suroviny pro výrobu NAD+. V těle se přirozeně vyskytuje pět takových prekurzorů: tryptofan, nikotinamid (Nam), kyselina nikotinová (NA nebo niacin), nikotinamid ribozid (NR) a nikotinamid mononukleotid (NMN). Z těchto všech představuje právě NMN jeden z finálních kroků syntézy NAD+.
Všechny tyto prekurzory získáváme ze stravy. Nam, NA a NR jsou formou vitaminu B3, což je významná živina. Jakmile se dostane do těla, dokážou naše buňky syntetizovat NAD+ několika různými cestami. Biochemická cesta je ekvivalentem výrobní linky v továrně. V případě NAD+ v našem těle běží několik takových výrobních linek souběžně, všechny vyrábějící jeden produkt.
První z těchto cest se nazývá cesta de novo. De novo je latinské označení, které znamená „znova, od základů.“ Cesta de novo začíná prvním z prekurzorů NAD+, tryptofanem, a od tohoto bodu pokračuje k vyšším stupňům.
Druhou cestou je cesta záchranná. Záchranná cesta je něco jako recyklace, při níž se NAD+ vytváří z produktů rozpadu NAD+. Všechny bílkoviny v těle se musí pravidelně rozkládat, aby se nehromadily, což by mohlo vést k problémům. Součástí tohoto cyklu je produkce a degradace, kdy si enzymy odeberou část toho, co zbude z rozpadu bílkovin a vrátí to rovnou zpět do výrobní linky produkující tu samou bílkovinu.
Biosyntéza NAD+ z NMN
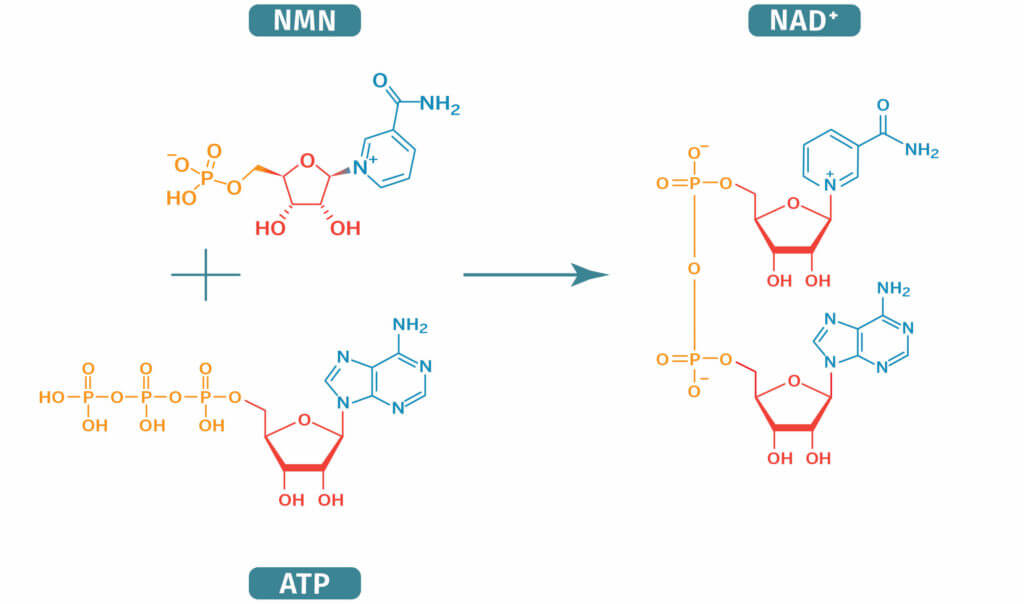
Jak se NMN v těle syntetizuje?
NMN se v těle vyrábí z vitaminů B. Enzym, který je odpovědný za výrobu NMN v těle, se nazývá nikotinamidfosforibosyltrasferáza (NAMPT). NAMPT naváže nikotinamid (vitamin B3) k fosfátu cukru zvanému PRPP (5’-fosforibozyl-1-pyrofosfát). NMN se může vyrábět také z „nikotinamidribozidu“ (NR) navázáním fosfátové skupiny.
„NAMPT“ je enzym limitující rychlost při výrobě NAD+. To znamená, že nižší koncentrace NAMPT způsobuje sníženou produkci NMN, což má za následek snížení hladiny NAD+. Přidáním molekul prekurzoru, jako je NMN, je možno produkci NAD+ zrychlit.
Metody zvyšování koncentrace NAD+
Držení půstu nebo snižování příjmu kalorií, tedy omezování kalorického příjmu, zvyšuje koncentraci NAD+ a aktivitu sirtuinů. U myší zvýšení koncentrace NAD+ a aktivity sirtuinů v důsledku snížení kalorického příjmu vedlo ke zpomalení procesu stárnutí. Ačkoli je NAD+ přirozeně obsažen v některých potravinách, jeho koncentrace jsou příliš nízké, aby měly vliv na koncentraci v buňkách. Užívání některých doplňků stravy, jako je například NMN, prokázalo účinek na zvýšení hladin NAD+.
Doplněk NAD jako NMN
Nitrobuněčné koncentrace NAD+ klesají v důsledku stárnutí s tím, jak normální buněčné funkce vyčerpávají zásoby NAD+ v průběhu času. Zdravé hladiny NAD+ se obnovují doplňováním prekurzorů NAD+. Na základě výzkumu víme, že prekurzory, jako je NMN a nikotinamid ribozid (NR) jsou považovány za doplňky podporující produkci NAD+ a zvyšující koncentraci NAD+. David Sinclair, vědec z harvardské univerzity, zabývající se výzkumem NAD+, tvrdí: „Užívání nebo podávání NAD+ přímo do organismu není praktickým řešením. Molekula NAD+ není schopna ihned překonat buněčné membrány a vstupovat dovnitř buněk, tudíž není k dispozici pro pozitivní ovlivnění metabolismu. Namísto toho lze přidat molekuly prekurzoru NAD+, které zvyšují koncentraci biologicky dostupného NAD+.“ To znamená, že NAD+ nelze užívat ve formě doplňku přímo, protože by nebyl snadno absorbován. Prekurzory NAD+ jsou však absorbovány snadněji než NAD+ a jsou tedy mnohem účinnějšími doplňky.
Jak jsou NMN doplňky absorbovány a distribuovány v těle?
NMN se zřejmě absorbuje do buněk prostřednictvím molekulárního transportéru, který se nachází na povrchu buňky. Protože je molekula NMN menší než molekula NAD+, je do buněk absorbována mnohem snadněji. NAD+ se do těla nedostává snadno, v cestě mu stojí bariéra představovaná buněčnou membránou. Membrána má bezvodý prostor, který zabraňuje vstupu iontů, polárních molekul a velkých molekul bez použití transportérů. Dříve se myslelo, že před vstupem do buňky se musí NMN upravit, avšak důkazy naznačují, že dokáže do buněk vstupovat přímo prostřednictvím specifického NMN transportéru obsaženého v buněčné membráně.
Injekční aplikací NMN bylo dosaženo zvýšení koncentrace NAD+ v různých částech těla, včetně sleziny, tukové tkáně, srdce, kosterních svalů, ledvin, varlat, očí a krevních cév. Ústní podávání NMN u myší zvyšuje koncentraci NAD+ v játrech již do 15 minut.
NMN se rychle převádí na NAD+
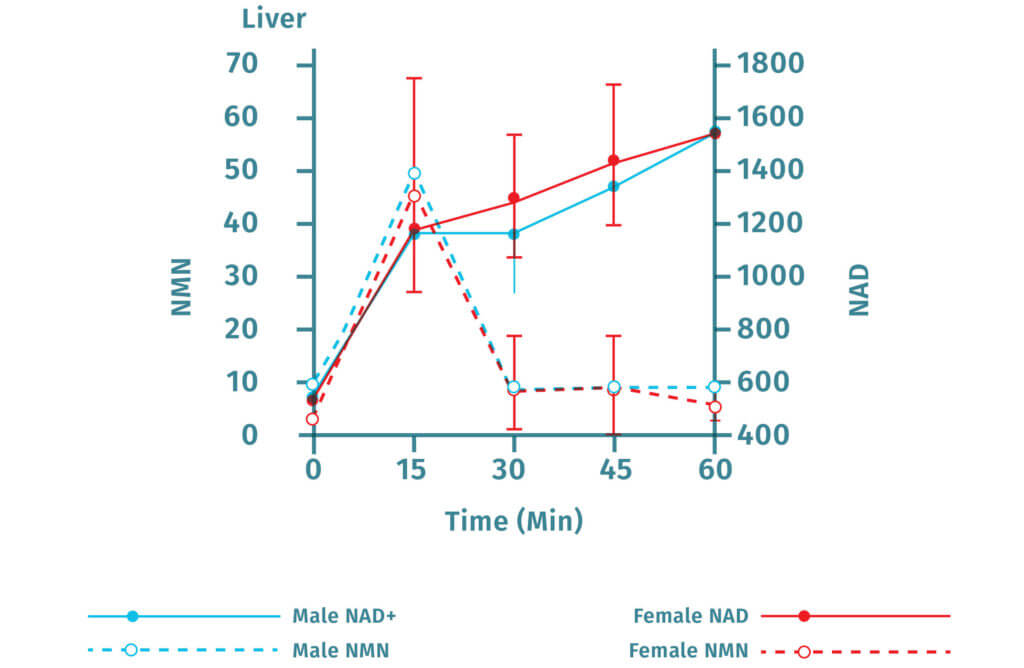
Popisky shora
- Játra
- Čas (min)
- Mužský NAD+
- Mužský NMN
- Ženský NAD+
- Ženský NMN
Vedlejší účinky a bezpečnost užívání NMN
NMN je považován za bezpečný u zvířat a na základě slibných výsledků byly zahájeny také klinické studie na lidech. Tato molekula je převážně považována za neškodnou a netoxickou, a to i ve vysokých koncentracích jak u myší, tak u člověka. Dlouhodobé (roční) podávání myším nemá žádné toxické účinky. Byla dokončena úplně první klinická studie na lidech a důkazy v ní získané podporují teorii, že v jednorázových dávkách není toxická ani u člověka.
Ačkoli jedna studie na japonských mužích, publikovaná v listopadu 2019, zjistila, že studované subjekty vykazovaly po podání NMN zvýšené hladiny bilirubinu v krvi, pohybovalo se toto zvýšení v rámci normálního rozsahu. V budoucnu se studie zaměří na dlouhodobou bezpečnost a efektivnost užívání. NMN není spojován s žádnými dalšími známými vedlejšími účinky.
Historie NMN a NAD+
Nikotinamiadenindinukleotid, zkráceně NAD, je jednou z nejdůležitějších a nejvšestrannějších molekul v našem těle. Protože je nezbytný pro zajišťování energie pro buňky, téměř žádné biologické procesy se bez něj neobejdou. V důsledku toho je NAD dlouhodobě cílem zájmu vědeckého výzkumů.
V roce 1906 objevili Arthur Harden a William John Young „faktor“ v tekutině extrahované z pivovarských kvasnic, která byla posílena fermentací cukru na alkohol. Tímto „faktorem“, tehdy nazvaným „koferment“, byl právě NAD.
Harden spolu s Hansem von Euler-Chelpinem pokračoval v odhalování tajemství fermentace. V roce 1929 získali Nobelovu cenu za dosažení podrobného porozumění těmto procesům, a to včetně chemického vzorce a vlastností toho, co později vešlo ve známost jako NAD.
Příběh NAD se dále rozvíjel ve 30. letech pod vedením Otto Warburga, dalšího laureáta Nobelovy ceny, který objevil ústřední roli NAD v mnoha biochemických reakcích. Warburg zjistil, že NAD funguje jako jakési biologické relé pro elektrony.
Přenos elektronů z jedné molekuly do druhé tvoří základ energie potřebné pro všechny biochemické reakce.
V roce 1937 Conrad Elvehjem a jeho kolegové z University of Wisconsin v Madisonu zjistili, že suplementace NAD+ vyléčila psy z onemocnění zvaného pelagra, tedy „černání jazyka“. U lidí pelagru provází celá řada symptomů, včetně průjmu, demence a boláků v ústech. Jejím důvodem je nedostatek niacinu a dnes se běžně léčí nikotinamidem, jedním z prekurzorů NMN. Výzkum NAD + Arthura Kornberga ve 40. a 50. letech byl zásadní pro poznání principů, které stojí za replikací DNA a transkripcí RNA, tedy dvou procesů nezbytných pro život.
V roce 1958 Jack Preiss a Philip Handler odhalili tři biochemické kroky, kterými se kyselina nikotinová přeměňuje na NAD. Tato série kroků, nazvaná cesta, je dnes známá jako Preiss-Handlerova cesta.
V roce 1963 Chambon, Weill a Mandel zjistili, že nikotinamid mononukleotid (NMN) dodává energii potřebnou k aktivaci důležitého enzymu buněčného jádra. Tento objev otevřel cestu sérii dalších významných objevů, týkajících se typu bílkoviny zvané PARP. PARP hraje klíčovou roli v opravě poškozené DNA, regulaci buněčné smrti, a její aktivita je spojována se změnami délky života.
V roce 1976 Rechsteiner a jeho kolegové objevili přesvědčivý důkaz, že NAD+ kromě své klasické biochemické role jako molekuly přenášející energii zastává také „některé další významné funkce“ v buňkách savců,
Tento objev umožnil Leonardu Guarentemu a jeho kolegům zjistit, že proteiny zvané sirtuiny využívají NAD pro prodloužení života specifickým „umlčováním“ některých genů.
Od té doby zájem o NAD a jeho meziprodukty, NMN a NR, stále vzrůstá, a to především pro jejich potenciál zmírňovat projevy celé řady problémů souvisejících s věkem.
Budoucnost nikotinamid mononukleotidu
Pro slibné terapeutické vlastnosti, které NMN prokázal ve studiích na zvířecích modelech, se nyní vědci snaží přijít na to, jak tato molekula funguje v lidském těle. Nedávná klinická studie v Japonsku demonstrovala, že molekula je bezpečná a v použitém dávkování dobře tolerovaná. Další studie na lidech se připravují nebo již probíhají. Je to fascinující a všestranná molekula, o které se toho máme ještě mnoho co učit.
Literatura
- 1. Vincenzo Carafa, Dante Rotili, Mariantonietta Forgione, Francesca Cuomo, Enrica Serretiello, Gebremedhin Solomon Hailu, Elina Jarho, Maija Lahtela-Kakkonen, Antonello Mai, Lucia Altucci. Sirtuin functions and modulation: from chemistry to the clinic. Clin epigenetics, 2016; DOI: 10.1186/s13148-016-0224-3.
- 2. Niels J. Connell, Riekelt H. Houtkooper, Patrick Schrauwen. NAD+ metabolism as a target for metabolic health: have we found the silver bullet? Diabetologia, 2019; DOI: 10.1007/s00125-019-4831-3.
- 3. Julia Evangelou. “Natural compound reduces signs of aging in healthy mice.” ScienceDaily.com. 27 October, 2016. Web. 16 January. 2020.
- 4. Henryk Jęśko, Przemysław Wencel, Robert P. Strosznajder, Joanna B. Strosznajder. Sirtuins and Their Roles in Brain Aging and Neurodegenerative Disorders. Neurochem Res, 2017; DOI: 10.1007/s11064-016-2110-y.
- 5. Ann Katrin-Hopp, Patrick Grüter, Michael O. Hottiger. Regulation of Glucose Metabolism by NAD+ and ADP-Ribosylation. Cells, 2019; DOI: 10.3390/cells8080890.
- 6. Vamshi K.C. Nimmagadda, Tapas K. Makar, Krish Chandrasekaran, Avinash Rao Sagi, Jayanta Ray, James W. Russell, Christopher T Bever Jr. SIRT1 and NAD+ precursors: Therapeutic targets in multiple sclerosis a review. J Neuroimmunol, 2017; DOI: 10.1016/j.jneuroim.2016.07.007.
- 7. Katalin Sas, Elza Szabó, László Vécsei. Mitochondria, Oxidative Stress and the Kynurenine System, with a Focus on Ageing and Neuroprotection. Molecules, 2018; DOI: 10.3390/molecules23010191.
- 8. Yue Yang, Anthony A. Sauve. NAD+ metabolism: Bioenergetics, signaling and manipulation for therapy. Biochim Biophys Acta, 2016; DOI: 10.1016/j.bbapap.2016.06.014.
- 9. Jun Yoshino, Kathryn F. Mills, Myeong Jin Yoon, Shin-ichiro Imai. Nicotinamide Mononucleotide, a Key NAD+ Intermediate, Treats the Pathophysiology of Diet- and Age-Induced Diabetes in Mice. Cell Metab, 2011; DOI: 10.1016/j.cmet.2011.08.014.
- 10. Mills KF, Yoshida S, Stein LR, Grozio A, Kubota S, Sasaki Y, Redpath P, Migaud ME, Apte RS, Uchida K, Yoshino J, Imai SI. Long-Term Administration of Nicotinamide Mononucleotide Mitigates Age-Associated Physiological Decline in Mice. Cell Metab, 2016; DOI: 10.1016/j.cmet.2016.09.013.
- 11. Shuang Zhou, Xiaoqiang Tang, Hou-Zao Chen. Sirtuins and Insulin Resistance. Front Endocrinol (Lausanne), 2018; DOI: 10.3389/fendo.2018.00748.
- 12. Irie J, Inagaki E, Fujita M, et al. Effect of oral administration of nicotinamide mononucleotide on clinical parameters and nicotinamide metabolite levels in healthy Japanese men, 2019 Nov 2]. Endocr J. 2019;10.1507/endocrj.EJ19-0313. doi:10.1507/endocrj.EJ19-0313
